医科2013.02.25 講演
[保険診療のてびき] ループ利尿薬をどう使うべきか?新しいエビデンスが示した方向とは?
兵庫医科大学ささやま医療センター 地域総合医療学講座 川端 正明先生講演
ループ利尿薬の使用量多いほど予後不良
ループ利尿薬は、心不全の治療薬として、ジギタリスに次ぐ長い歴史を誇る薬である。ジギタリスが心不全治療に占める役割は、昔と比べてはるかに小さくなっているが、ループ利尿薬はうっ血症状をコントロールするために、今も広く使用されている。しかし、古くから不可欠な薬剤として使用されてきたがゆえに、質の高いエビデンスが皆無といってよい状況にある。
むしろ、レトロスペクティブな検討からは、ループ利尿薬の使用量が多いほど、患者の予後が悪いということが明らかになってきた。もちろん、重症な患者ほど大量のループ利尿薬が必要だから、予後不良であるというのは当然である。しかし、一般に知られている心不全の重症度の指標で補正してもループ利尿薬の使用量が多いことが、有意な予後不良因子であることが報告されている。
ループ利尿薬による神経体液性因子活性化を防ぐために
それではループ利尿薬は、どのようにして慢性心不全患者の予後を悪化させているのだろうか。その機序として最も注目されるのは、レニン・アンジオテンシン(RA)系や交感神経系などの神経体液性因子の活性化である。ループ利尿薬は体液量の減少だけでなく、密集斑細胞への直接作用によりレニン分泌を刺激し、RA系を活性化させる。
それでは、ループ利尿薬による神経体液性因子の活性化を防ぐためには、どうすればいいだろうか。まず、ループ利尿薬の用量を最小限にすることが望ましい。そのためには漫然と投与せず、心不全が安定していれば臨床症状や体重をモニターしながら、慎重に減量していく。
次に、ACE阻害薬、ARB、β遮断薬、アルドステロン受容体拮抗薬などの神経体液性因子抑制薬を、十分量使用する必要がある。
短時間作用型より長時間作用型ループ利尿薬が好ましい
そしてもう一つ、われわれが考えたのは長時間作用型ループ利尿薬を使用することである。その発想の元となったのは、1995年の「カルシウム拮抗薬論争」である。Furbergらのグループが、Ca拮抗薬を虚血性心疾患患者や高血圧患者に使用した論文のメタアナリシスを行い、Ca拮抗薬が心筋梗塞の発症を増やすと報告し、問題となった。その後、これらの危険性は短時間作用型のCa拮抗薬に限られ、長時間作用型Ca拮抗薬ではこのような現象は見られないことが明らかになった。
短時間作用型Ca拮抗薬は、急激な降圧に伴って交感神経活性を亢進させ、心拍数や心仕事量を増加させ虚血性心疾患の悪化を招くのであろうと結論され、短時間作用型Ca拮抗薬の使用は激減した。
一方、現在使用されているループ利尿薬の多くは、短時間作用型のフロセミドである。利尿薬も体液量減少や血圧の低下に伴い、RA系や交感神経系の活性化を伴うのであるから、短時間作用型よりも長時間作用型の方がよい可能性がある。
Yoshidaらは、Dahl食塩感受性高血圧ラットに高食塩食を負荷することにより誘発された心不全モデルにおいて、短時間作用型のフロセミドは予後を改善しないが、長時間作用型のアゾセミドは心臓交感神経活性を低下させるとともに、予後も改善することを示した。このことは、ループ利尿薬も長時間作用型の方が好ましいことを示唆している。
長時間作用型と短時間作用型ループ利尿薬の優劣
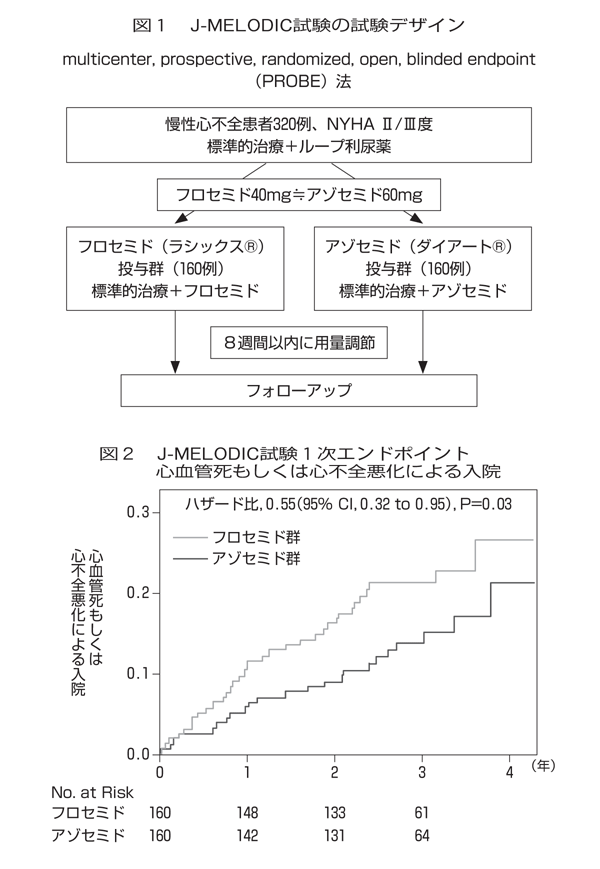
われわれは、長時間作用型ループ利尿薬と短時間作用型ループ利尿薬の優劣を明らかにするため、「利尿薬のクラス効果に基づいた慢性心不全に対する効果的薬物療法の確立に関する多施設共同臨床研究[Japanese Multicenter Evaluation of LOng-versus short-acting Diuretics In Congestive heart failure(J-MELODIC)]を実施した。(図1、2)対象はNYHA Ⅱ-Ⅲの症例で、1カ月以上安定している慢性心不全(左室駆出率は問わない)でループ利尿薬(フロセミド、アゾセミド、もしくはトラセミド)が投与されている患者である。文書にて同意の得られた患者をアゾセミド群(ループ利尿薬をアゾセミド錠1日1回朝食後30㎎〜60㎎経口投与のみとする。120㎎まで増量可)とフロセミド群(ループ利尿薬をフロセミド錠1日1回朝食後20㎎〜40㎎経口投与のみとする。80㎎まで増量可)に無作為に割付け、PROBE(Prospective, Randomized, Open, Blinded-Endopoint design)法にて最低2年間観察追跡を行った。
1次エンドポイントは心不全症状の悪化による入院または心血管死であり、2次エンドポイントは(1)全死亡、(2)QOLの悪化、(3)BNPの上昇、(4)心不全入院もしくは心不全症状の悪化による薬剤の変更・追加である。左室駆出率を問わずにエントリーしたため、J-MELODIC試験に登録された患者には、左室駆出率の保たれた心不全(Heart failure with preserved ejection fraction)が多く、左室駆出率の平均値が50%を超えているのが特徴である。
最低2年間のフォローアップの結果、1次エンドポイントの心不全症状の悪化による入院または心血管死は、アゾセミド群で有意に少なかった(ハザード比0.55、95%信頼区間0.32-0.95、P=0.03)。2次エンドポイントの心不全入院もしくは心不全症状の悪化による薬剤の変更・追加も、アゾセミド群で有意に少なかった(ハザード比0.60、95%信頼区間0.36-0.99、P=0.048)。
以上より、ラットの心不全モデルと同様に、慢性心不全患者においても、長時間作用型ループ利尿薬の方が短時間作用型ループ利尿薬よりも予後を改善することが明らかになった。
(2012年11月17日薬科部研究会より、中見出しは編集部)