医科2025.06.15 講演
第57回総会記念講演より
感染症に立ち向かうこれからの免疫学
-COVID-19で分かったこと、わからなかったこと-(2025年6月15日)
大阪大学感染症総合教育研究拠点 准教授 香山 雅子先生講演
2019年末に出現したSARS-CoV-2による世界的パンデミックは、社会、医療体制の在り方など世界中の人々の暮らしに大きな影響を与えたが、一方でヒト免疫学の理解を飛躍的に高めることにもなった。2020年以降、人類が初めて遭遇するウイルス、初めて実用化されたmRNAワクチンに対するヒト免疫応答が世界規模で同時に解析されたからである。
その中でわれわれが改めて認識したのは、記憶免疫の重要性であり、ヒト免疫系の複雑性である。感染・ワクチンで誘導される記憶免疫は感染防御の基幹であることがヒトサンプルの解析からも実証された。一方で、動物実験とは異なり、ヒトでは発症、重症度、副反応、後遺症の程度も個体によって大きく異なることも示された。
コロナパンデミックを通して得られた記憶免疫の知見、ワクチンの課題を総括するとともに、今後の免疫学研究の展望についても触れたい。
1)免疫記憶について
感染防御において、中心的な役割を担うのが獲得免疫の記憶応答である。ウイルスなどの病原体に感染すると、この病原体に特異的なB細胞が活性化され、中和抗体を産生するプラズマ細胞に分化する。プラズマ細胞の一部は骨髄で長期生存し、中和抗体を供給し続ける。また、一部のB細胞はメモリーB細胞として体内に残存し、再感染時の迅速な抗体産生を可能にする。ウイルスに感染した細胞を直接破壊するCD8+T細胞や、抗体産生を助けるCD4+T細胞も記憶T細胞として長期間体内に残り、次の感染に対して即時応答を可能にする。COVID-19のパンデミックでは、獲得免疫の質と持続性が、感染防御や重症化予防において重要であることも明らかになった。記憶免疫の質とは、単に記憶細胞の数のことではなく、これらの細胞が機能的につまり異物に対して迅速かつ強力に反応できるかどうかを意味する。
感染やワクチン接種によって誘導される記憶B細胞の持つ抗体分子がウイルス抗原に対して十分な親和性を持つか、あるいは変異ウイルス抗原にも交差反応性を示すかどうかが、再感染時の病原体排除の鍵となる。また記憶T細胞のサイトカイン産生能や細胞傷害活性能も重要な要素の一つである。免疫記憶の持続性も重要である。
感染、ワクチン接種後のウイルス特異的抗体価、記憶T、B細胞数の変化をlongitudinalに解析した研究結果から、特異的抗体は数カ月で減少するのに対し、SARS-CoV-2特異的記憶T細胞は一定数維持されることが明らかとなった。抗体価が減少してもT細胞応答が比較的安定に維持されている場合は、重症化を防ぐ防波堤として機能していると考えられている。
また、自然感染によって獲得された免疫記憶と、ワクチンによる免疫記憶を併せ持ついわゆるハイブリッド免疫は、より持続性と幅広さに優れていることが示唆されている。ハイブリッド免疫を持つ個体では、記憶免疫細胞、抗体価が維持されやすく、また抗体の交差反応性も優れていることが報告されている。
一方で、COVID-19の流行を契機に、自然免疫にも「記憶」に相当する現象が存在することが注目された。これは訓練免疫(trained immunity)と呼ばれる現象で、自然免疫に関与する単球・マクロファージ・NK細胞などの細胞において、初回の病原体刺激によりエピジェネティックおよび代謝的な変化が起こり、以降の感染に対して強化された応答を示すというものである。
獲得免疫のような抗原特異性は持たないが、異なる病原体に対しても交差的な防御効果を持つ点で、非特異的な"自然免疫の記憶"として機能すると理解されている。この現象は病原体非特異的な感染防御の強化を実現する新たな免疫制御機構として注目されているが、訓練免疫の過剰活性化はサイトカインストームのような病的炎症を引き起こすリスクを伴う。
訓練免疫の誘導・維持・制御に関しては不明な点が多く残されており、今後詳細な解析が必要である。
2)mRNAワクチン
COVID-19パンデミックを通じて、mRNAワクチンの有効性・迅速性・柔軟性が実証された。mRNAワクチンは、標的抗原をコードするmRNAを細胞内に導入し、抗原が細胞内で合成されることで、自然免疫と獲得免疫を同時に活性化する。抗体応答とT細胞応答の両方を強力に誘導できるという利点を持ち、感染予防・重症化抑制において高い有効性を発揮した。
また、mRNA配列を迅速に変更できるという柔軟性から、ウイルス情報が得られたら短期間で変異株への対応が可能である点も、従来のワクチン技術にはない特長である。
ただしSARS-CoV-2はスパイク蛋白の抗原性が変異によって容易に変化し、既存の抗体では中和できない"免疫逃避"変異を繰り返す。こうした個別の変異に追随するワクチン戦略には限界があるため、抗原の保存領域(変異しにくい部分)を標的とし、ウイルスの変異にも対応し免疫を誘導できるユニバーサルワクチン開発が期待されている。
3)免疫応答の個体差
COVID-19では、免疫応答における個体差の重大性が浮き彫りになった。感染しても無症状な人もいれば、若年健常者でも急速に重症化する例も存在した。また、mRNAワクチン接種後の副反応の強さや持続期間の違いにも大きな個体差があり、実験動物とは違うヒト免疫系の複雑性が再認識された。さらに注目されるのが、いわゆるコロナ後遺症(Long COVID)である。これは感染後数カ月以上にわたり続く倦怠感、呼吸苦、認知障害などの症状を指すものであり、やはりその発症にも個体差が認められている。
コロナ後遺症の免疫学的要因として、ウイルスの残存説、ウイルス感染をきっかけに自己免疫応答が誘導されている可能性、持続的なサイトカインの産生といった免疫系の慢性的な活性化、腸内細菌叢の異常などが言われており、どれか一つが単独で原因になっているというよりも、複数の要素が重なっていると考えられている。
今後コロナ後遺症動物モデルでの詳細なメカニズム解析、治療法開発が求められる。またヒトでの発症、重症度、後遺症と相関する因子、予測可能な因子を同定し、治療やワクチン開発に生かしていくことが重要な課題である。
以上のように、COVID-19はヒト免疫学の理解を飛躍的に進展させたと同時に、多くの未解決問題が残された。記憶免疫の多様性解明、mRNA技術のさらなる発展、そして個体差を前提とした免疫医療の構築は、今後の感染症対応だけでなく、自己免疫疾患、がん、老化など幅広い医学領域へ貢献することが期待される。
(6月15日、第57回総会記念講演より)
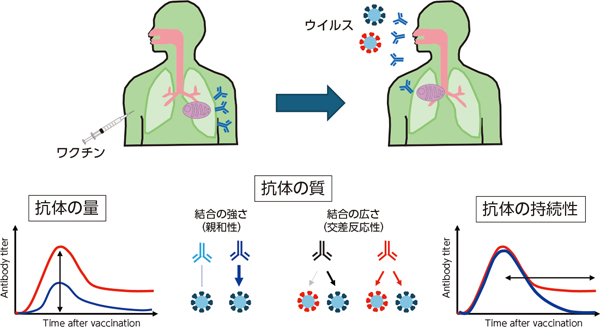
図 ワクチンで誘導される抗体応答の3つの重要な要素